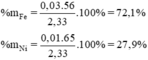Ngâm 2,33 gam hợp kim Fe – Zn trong dung dịch HCl đến phản ứng hoàn toàn thấy giải phóng 896 ml khí H2(đktc). Thành phần % của hỗn hợp là phương án nào sau đây.
A. 27,9% Zn và 72,1% Fe.
B. 26,9% Zn và 73,1% Fe.
C. 25,9% Zn và 74,1% Fe.
D. 24,9% Zn và 75,1% Fe.




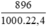 = 0,04(mol)
= 0,04(mol)